子科生物报道:北京时间2021年9月27日,中国科学院上海药物研究所李亚平课题组以“T lymphocyte membrane-decorated epigenetic nanoinducer of interferons for cancer immunotherapy”为题在国际顶级期刊Nature Nanotechnology在线发表了工程化T淋巴细胞膜修饰干扰素(IFN)表观遗传纳米诱导剂改善肿瘤免疫治疗的最新研究成果。该团队创造性地设计构建了一种“精准递送+智能释药一体化”的仿生纳米囊泡,揭示了该纳米递药系统的作用机理,取得了肿瘤特异性IFN诱导并同时克服免疫耐受的重大突破。
免疫疗法是肿瘤治疗领域的革命性进展,肿瘤内I型IFN的水平与包括结肠癌、黑色素瘤和三阴性乳腺癌等在内的多种肿瘤预后密切相关。虽然目前临床上可以通过注射重组人IFN提高其瘤内水平,但其肿瘤靶向性差、疗效低,而且易产生明显的全身免疫毒性。化疗药物、分子靶向药物以及表观遗传药物虽然也能一定程度上诱导肿瘤内IFN表达,但由于特异性差,效果并不理想,特别是瘤内IFN的上调会不可避免地诱导多种免疫检查点分子表达,促使肿瘤发生免疫逃逸进而产生免疫耐受。因此,如何选择性提高瘤内IFN等免疫分子水平,并同时克服其诱导的免疫耐受,是肿瘤免疫治疗领域亟待解决的一个重大科学问题。
针对上述临床重大需求,上海药物所张鹏程研究员、李亚平研究员团队首先通过基因工程技术构建了高表达程序性死亡受体-1(PD1)的T细胞,并获得该工程化细胞的膜囊;随后用其包裹负载赖氨酸特异性组蛋白去甲基化酶1(LSD1)抑制剂ORY-1001的白蛋白纳米粒; 最后以还原敏感穿膜肽M70对其进行表面修饰获得表观遗传调控纳米囊泡(OPEN)(图1A)。静脉注射后,OPEN通过受配体(PD1/PDL1)的识别,主动靶向递送ORY-1001至表达PDL1的肿瘤细胞,在胞内谷光甘肽(GSH)的作用下快速释放ORY-1001,上调IFN表达, 促进抗原递呈细胞(APCs)活化和抗原呈递, 活化细胞毒性T淋巴细胞(CTLs),增加肿瘤微环境内T细胞浸润,同时阻断原有以及IFN上调的多种免疫检查点配体介导的免疫逃逸(图1B)。
研究数据显示,OPEN能特异性靶向肿瘤,高效诱导瘤内IFN分泌,上调肿瘤细胞PDL1和主要组织相容性复合体-I(MHC-I)等的表达,并进一步促进OPEN摄取,产生自增强效应,将瘤中CTLs浸润增加了29倍,显著降低ORY-1001的免疫副作用(图1C),在动物模型上有效抑制三阴性乳腺癌、黑色素瘤或结肠癌的生长(图1D)。该研究开拓了精准递送+智能释药一体化技术调控表观遗传、克服免疫耐受、改善肿瘤免疫治疗的新方向,为提高包括IFN在内的兼具抗癌活性和促进免疫逃逸的活性分子疗效以及降低其免疫副作用提供了新思路。
上海药物所博士研究生翟艺慧和上海交通大学仁济医院博士研究生王金名为该论文第一作者,上海药物所李亚平研究员和张鹏程研究员为论文共同通讯作者。上海交通大学朱鹤研究员,国家蛋白质科学中心(上海)于洋研究员和王研科工程师,中科环渤海(烟台)药物高等研究院和烟台药物所荣荣博士、孔颖工程师,上海药物所博士后郎天群及研究生蔡颖、冉伟、熊凤琴和郑超等参与相关研究工作,该工作还得到了上海交通大学邓刘福研究员和上海药物所王江研究员的帮助。研究工作同时得到了国家自然科学基金、中国科学院青年创新促进会和山东省自然科学基金的支持。
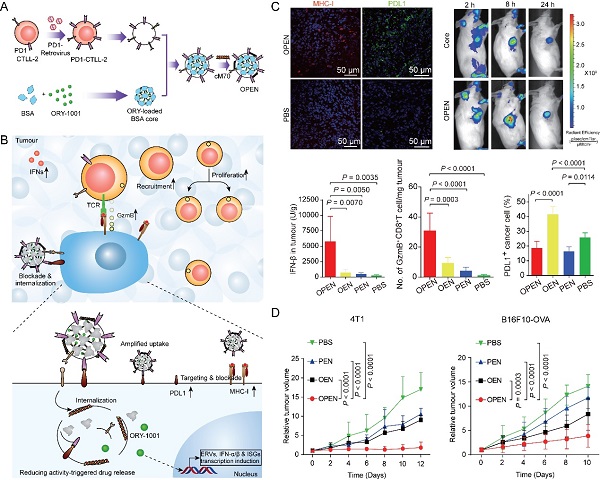
图1:(A). PD1过表达CTLL-2细胞的构建和负载ORY-1001纳米囊泡(OPEN)的制备。(B). OPEN被肿瘤细胞PDL1识别并入胞,上调IFN表达,增加肿瘤微环境内T细胞浸润并促进CTL活化,同时阻断PDL1介导的免疫逃逸。(C). OPEN特异性靶向肿瘤,显著上调瘤内IFN表达,促进抗原递呈,提高肿瘤中细胞毒性T细胞浸润并有效解除ORY-1001造成的免疫抑制。(D). OPEN显著抑制乳腺癌和黑色素瘤的生长。