子科生物报道:4月12日,基础医学院程金科教授实验室在Cell Reports发表了题为“SENP1-Sirt3 signaling promotes α-ketoglutarate production during M2 macrophage polarization” 的研究论文,报道了SENP1-Sirt3信号轴通过调控谷氨酰胺代谢促进α酮戊二酸产生和巨噬细胞M2型极化的新机制。

巨噬细胞是机体固有免疫系统重要成员之一,参与病原体识别和清除,抗原递呈和T细胞活化,启动组织损伤修复以及调控代谢和肿瘤等疾病的微环境稳态。巨噬细胞在不同的信号激活后形成不同的活化状态,典型的有促进炎症反应的M1型和抑制炎症反应的M2型。M1型巨噬细胞主要通过产生活性氧和活性氮以及诸多促炎因子,清除病原体、凋亡/坏死细胞和肿瘤细胞,是经典的巨噬细胞活化形式;而M2型巨噬细胞由于能够抑制炎症和免疫反应,在组织损伤修复和抗肿瘤免疫调控等方面有重要作用,近年来倍数关注。对于调控巨噬细胞M2型极化的信号通路有许多研究,但由于其复杂性,到目前依然有许多调控分子与作用机制未解。
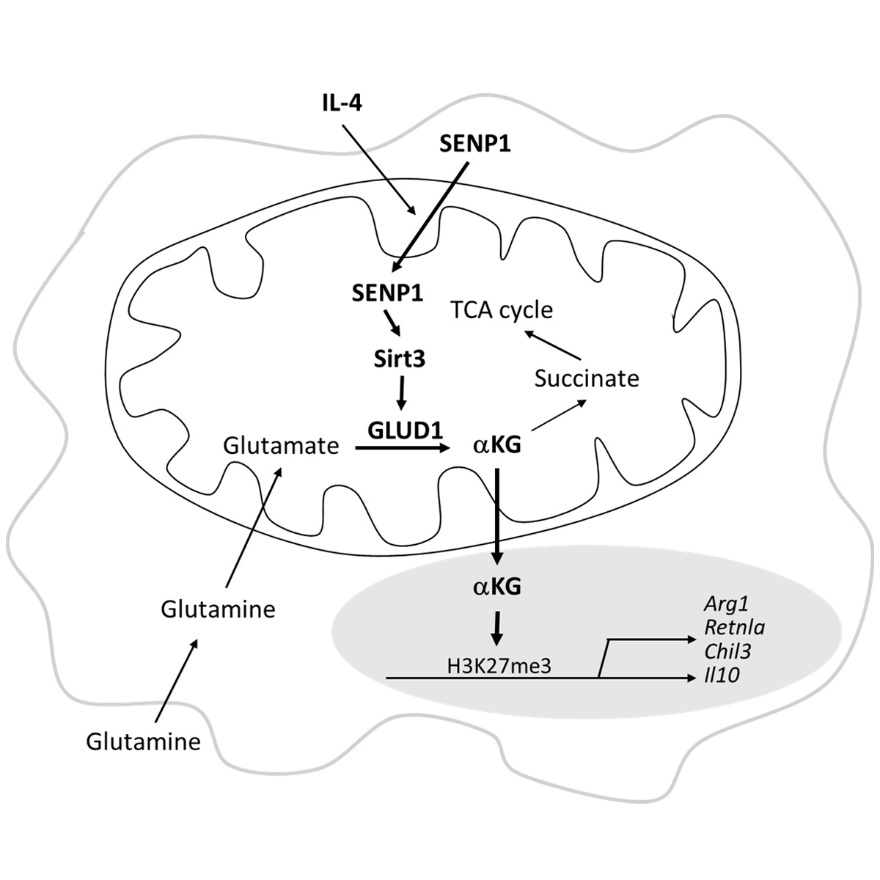
程金科教授实验室于2019年报道了SENP1-Sirt3轴在细胞线粒体代谢应激反应中的关键调控作用,是细胞代谢可塑性和细胞稳态维持的重要信号通路(MolecularCell, 2019)。SENP1-Sirt3轴通过调控脂肪酸氧化磷酸化代谢促进记忆性T细胞形成和活化,在抗肿瘤免疫中有重要作用(NatureCommunication,2021)。在这些研究的基础上,博士研究生周炜等进一步探讨了这一通路在巨噬细胞活化过程中的作用。他们发现SENP1-Sirt3 信号轴活化特异性地促进IL-4诱导的巨噬细胞M2型活化。通过代谢组学和基因组学的分析,发现这一通路调控了谷氨酰胺分解代谢途径中催化谷氨酸转化为α酮戊二酸的谷氨酸脱氢酶(GLUD1)的活性,促进了α酮戊二酸的产生。α酮戊二酸是一个关键的表观遗传调控因子,能够促进巨噬细胞M2型极化。因此,这一研究发现了SENP1-Sirt3轴对谷氨酰胺代谢和α酮戊二酸产生的新调控机制和这一机制对巨噬细胞M2型极化的调控作用。 这一发现可能为探讨肿瘤代谢微环境如何影响抗肿瘤免疫提供新的思路和干预途径。
该研究主要由博士研究生周炜来完成,博士研究生胡高磊参与了部分工作。该项目得到了国家自然科学基金和上海市教委科研创新计划项目等基金的资助。同时,该研究还得到了上海交通大学医学院附属仁济医院泌尿科的薛蔚教授的指导和大力支持。薛蔚教授和程金科教授为该论文的共同通讯作者。